RetroNectin Recombinant Human Fibronectin Fragment, 2.5 mg
R$13.352,25
pesquisa usando células hematopoiéticas e outras células em suspensão tem sido limitada em parte pela baixa eficiência da transferência de genes (transdução e transfecção) para esses tipos de células. O reagente RetroNectin promove a colocalização de lentivírus ou retrovírus com células-alvo para aumentar drasticamente a eficiência da transdução. Como consequência, o reagente RetroNectin é agora o melhorador de transdução padrão-ouro para transferência de genes retrovirais/lentivirais para células hematopoiéticas e é uma grande promessa na aplicação clínica, tendo sido usado em mais de 40 ensaios clínicos.
Disponível por encomenda
Visão geral
- Eficiência aprimorada de transferência de genes para transdução retroviral ou lentiviral de células em suspensão, células-tronco hematopoiéticas e outros tipos de células difíceis de infectar
- Menos toxicidade do que outros potenciadores de transdução comumente usados, incluindo polibreno e protamina
- Peptídeo totalmente recombinante
- Gato. # T110A consiste em dez placas de 35 mm pré-revestidas com reagente RetroNectin
- A eficiência da expansão das células T (CD8+) pode ser significativamente aumentada na presença do reagente RetroNectin
- T202, grau RetroNectin® GMP, é fabricado e testado de acordo com as seguintes diretrizes, “Padrões para Controle de Fabricação e Controle de Qualidade, etc. de Produtos de Investigação (Produtos de Investigação GMP)” notificados pelo Ministério da Saúde e Bem-Estar do Japão (“PFSB Notificação nº 0709002, 9 de julho de 2008)” (PFSB: Agência de Segurança Farmacêutica e Alimentar)
- Takara Bio Inc., enviou um arquivo mestre de medicamentos (número de pedido DMF 18898) à Food and Drug Administration para o grau RetroNectin GMP.
Mais Informações
Formulários
- Transdução mediada por retroviral ou lentiviral aprimorada de células que expressam VLA-4 ou VLA-5 (incluindo muitos tipos de células hematopoiéticas)
- Expansão de células T in vitro de células CD8+
- O reagente RetroNectin foi usado em mais de 40 ensaios clínicos
- RetroNectin de grau de pesquisa (Cat. # T100A/B; T110A): Apenas para uso em pesquisa. Não deve ser usado em procedimentos diagnósticos ou terapêuticos.
- RetroNectin de grau GMP (Cat. # T202): Fabricado como um produto de qualidade garantida, de acordo com as diretrizes relevantes das Boas Práticas de Fabricação (BPF). Este produto pode ser usado para aplicações clínicas ex vivo .
Para outras aplicações além do uso em pesquisa
- O método de expansão de células T por estimulação de RetroNectin requer uma licença da Takara Bio Inc. para outros usos além da pesquisa . Entre em contato com bio-licensing@takara-bio.co.jp para obter detalhes.
- O grau RetroNectin GMP pode ser usado para aplicações clínicas ex vivo (somente para uso em investigação): Para grau GMP, preencha e devolva este formulário antes da compra.
Informações adicionais do produto
Consulte o Certificado de Análise do produto para obter informações sobre as condições de armazenamento, componentes do produto e especificações técnicas. Consulte a Lista de componentes do kit para determinar os componentes do kit. Os Certificados de Análise e as Listas de Componentes do Kit estão localizados na guia Documentos.
Produtos relacionados
-
R$4.232,25
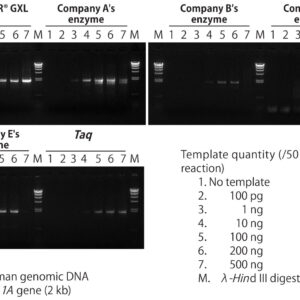
Uma enzima PCR de alta fidelidade e inicialização hotstart, a PrimeSTAR GXL DNA Polymerase se destaca em reações com modelos ricos em GC, modelo em excesso e amplicons longos de até 30 kb (GXL). A polimerase é fornecida com tubos separados de tampão otimizado (Mg 2+ plus) e dNTPs.
-
R$20.064,00
O Advantage 2 Polymerase Mix é uma mistura otimizada de enzimas PCR que é um equilíbrio comprovado de alto rendimento e alta fidelidade (com fidelidade 3X maior que a Taq normal ) para amplificação de cDNA e construção de biblioteca. Com um recurso de inicialização automática automática, nosso Advantage 2 Polymerase Mix pode amplificar prontamente uma ampla variedade de modelos de DNA, incluindo modelos longos de até 18 kb e DNA genômico complexo de até 6 kb.
A taq inclui dois buffers otimizados. dNTPs precisam ser adquiridos separadamente. -
R$5.215,50
O EmeraldAmp GT PCR Master Mix é uma versão com adição de corantes do EmeraldAmp MAX PCR Master Mix que é otimizada para ótimo desempenho e conveniência em aplicativos PCR padrão e de alto rendimento . Esta mistura principal inclui um tampão otimizado, enzima PCR, mistura dNTP, corante de carregamento de gel (verde) e um reagente de densidade em formato de pré-mistura 2X. Basta adicionar primers e modelo de DNA. Após a PCR, os amplicons podem ser usados diretamente de várias maneiras.
O conteúdo do tubo de PCR pode ser carregado diretamente em um gel de agarose para eletroforese ou usado diretamente em aplicações a jusante, como digestão de enzimas de restrição, clonagem de TA e sequenciamento direto. O EmeraldAmp GT PCR Master Mix pode ser usado para amplificar alvos genômicos de até ~5 kb e é compatível com alvos ricos em GC e AT.
-
RHB-Basal é um meio basal patenteado, definido e isento de soro, especificamente formulado para a propagação e diferenciação de células NS aderentes. RHB-Basal não contém quaisquer fatores de crescimento ou suplementos neuronais. Portanto, os clientes podem adaptar o RHB-Basal para atender aos requisitos específicos de seu tipo de célula pela adição de suplementos preferidos.